青年科學(xué)工作者論壇2008年第1期
《衛生研究》--2008年第一期 瘦素抵抗肥胖大鼠脂肪組織SOCS-3、PPARγ及ACO mRNA水平的探討
論著(zhù)
瘦素抵抗肥胖大鼠脂肪組織SOCS-3、PPARγ及ACO mRNA水平的探討
劉莉 顧海倫[1] 趙越 于飛 任亞浩 馬爽 陳麗麗 楊軍
中國醫科大學(xué)公共衛生學(xué)院營(yíng)養與食品衛生教研室,沈陽(yáng) 110001
摘要:目的 觀(guān)察高脂飲食誘導的肥胖瘦素抵抗大鼠細胞因子信號轉導抑制因子-3(SOCS-3)、過(guò)氧化物酶體增殖物激活受體γ(PPARγ)及乙酰輔酶A氧化酶(ACO)mRNA表達水平的變化。方法 30只Wistar雄性大鼠,6只為對照組喂飼基礎飼料,24只為高脂組喂飼高脂飼料,第8周末按體重增量從高脂組中篩選出8只大鼠作為肥胖組,測定對照組和肥胖組大鼠血清瘦素,附睪脂肪組織中SOCS-3,PPARγ以及ACO mRNA表達。結果 肥胖組大鼠體重以及血清瘦素水平均顯著(zhù)高于對照組(P<0.05);肥胖組脂肪組織SOCS-3、PPARγ mRNA水平顯著(zhù)高于對照組(P<0.05),而ACO mRNA則顯著(zhù)低于對照組(P<0.05)。結論 高脂飲食誘導的肥胖大鼠存在瘦素信號轉導通路的抑制,脂肪酸氧化能力降低,脂肪合成能力增強。
關(guān)鍵詞:肥胖 瘦素抵抗 信號轉導抑制因子-3 過(guò)氧化物酶體增殖物激活受體γ 乙酰輔酶A氧化酶
中圖分類(lèi)號: 文獻標識碼:A
Study on SOCS-3, PPARγ and ACO mRNA expression of adipose tissues in obese rats with leptin resistance
LIU Li, GU Hailun, ZHAO Yue, YU Fei, et al.
School of Public Health, China Medical University, Shenyang 110001, China
Abstract: Objective To study the difference of suppressor of cytokine signaling 3(SOCS-3), peroxisome proliferators-activated receptor-γ(PPARγ) and acyl-CoA oxidase (ACO) mRNA expression in obese rats with leptin resistant induced by high-fat diet. Methods 6 Wistar male rats were fed with basic diet as control, and 24 rats were fed with high-fat diet as high-fat diet group. At the end of the 8th week, 8 obese rats were selected by body weight from high-fat diet group as obese group. Serum leptin, SOCS-3, PPARγ and ACO mRNA of epididymal adipose tissues were detected. Results Compare to control, body weight, serum leptin, SOCS-3 and PPARγ mRNA expression significantly increased in obese group, but ACO mRNA markedly decreased in obese group. Conclusion Obese rats induced by high-fat diet showed the suppression of leptin signaling transduction pathway, decreasing fatty acid oxidation and increasing fat synthesis.
Key words: obesity, leptin resistance, suppressor of cytokine signaling 3, peroxisome proliferators-activated receptor-γ(PPARγ), acyl-CoA oxidase (ACO)
目前肥胖的發(fā)病率正逐年增加,它是糖尿病、高血壓、動(dòng)脈硬化等慢性疾病的重要危險因素。肥胖的病因復雜,研究顯示,大多數肥胖者和嚙齒類(lèi)動(dòng)物存在明顯的瘦素抵抗,而瘦素在中樞和外周的信號轉導通路缺陷,形成瘦素信號轉導抑制物的增多與瘦素抵抗的產(chǎn)生關(guān)系密切。本研究通過(guò)建立高脂飲食誘導的肥胖大鼠模型,檢測血清瘦素水平,脂肪組織中細胞因子信號轉導抑制因子-3(suppressor of cytokine signaling 3,SOCS-3),參與脂肪細胞分化及脂肪合成的過(guò)氧化物酶體增殖物激活受體γ(peroxisome proliferators-activated receptor-γ,PPARγ)以及脂肪酸氧化相關(guān)酶-乙酰輔酶A氧化酶(acyl-CoA oxidase,ACO)在脂肪組織中的mRNA表達情況,探討瘦素抵抗的肥胖大鼠中SOCS-3、PPARγ及ACO mRNA表達水平的變化。
1 材料與方法
1.1 動(dòng)物來(lái)源
30只Wistar雄性大鼠,體重(150±10)g,購于中國醫科大學(xué)實(shí)驗動(dòng)物中心。
1.2 試劑及試劑盒
大鼠瘦素ELISA試劑盒購于Biosource。PCR逆轉錄試劑盒購于TaKaRa大連寶生物公司, RNA提取采用天澤基因有限公司的RNAout, DNA Marker 采用TaKaRa的100bp DNA ladder
1.3 實(shí)驗方法
1.3.1 動(dòng)物實(shí)驗方法 大鼠適應性喂養1周,然后按體重隨機分為2組,對照組6只喂飼普通基礎飼料,高脂組24只喂飼高脂飼料,高脂飼料含基礎飼料73%、豬油20%、酪蛋白7%。大鼠單籠飼養,動(dòng)物室溫度(22±5)℃,相對濕度為(45±10)%,光照12h,自由攝取食物和水,共喂養8周,體重每周記錄一次。第8周末,按體重增量大于對照組體重增量加上1倍標準差作為肥胖標準,從高脂組篩選出8只肥胖大鼠為肥胖組,其余高脂組大鼠剔除不用。處死前禁食12h,乙醚麻醉后,腹主動(dòng)脈取血,靜置后離心取上清,-20℃保存待測,隨即取腎周、附睪、腸系膜脂肪墊稱(chēng)重,并立即將附睪脂肪墊放入液氮中,-80℃保存待測。
1.3.2 大鼠血清瘦素檢測 按ELISA試劑盒說(shuō)明書(shū)進(jìn)行,每個(gè)樣品做3個(gè)復孔,取平均值。
1.3.3 RT-PCR檢測脂肪組織SOCS-3 mRNA、PPARγmRNA、ACO mRNA表達 用RNAout提取大鼠附睪脂肪組織總RNA。調每個(gè)樣品的總RNA量為1μg。RT-PCR按照試劑盒使用方法:逆轉錄用15μl反應體系進(jìn)行,其中包括3μl的總RNA、MgCl2 3μl、10´RT Buffer 1.5μl、RNase Free dH2O 4.125μl、dNTP(各10mmol/L)1.5μl、RNase Inhibitor 0.375μl、AMV Reverse Transcriptase 0.75μl、Random 9 mers 0.75μl。
PCR反應用2μl cDNA進(jìn)行擴增(β-actin作為內參對照),加入10μl PCR反應體系中,包括5´PCR Buffer 2.5μl、滅菌蒸餾水7.16μl、TaKaRa Ex Taq HS 0.04μl、0.125μl上下游引物。方法如下:首先94℃預變性2min;PCR擴增35個(gè)循環(huán)包括94℃變性30s、53~56℃退火30s(溫度因不同基因而異)、72℃延伸1min。2%瓊脂糖電泳檢測PCR產(chǎn)物。Fluorchem V2.0 Stand Alone系統檢測PCR產(chǎn)物灰度值。PCR擴增上游和下游引物核酸序列見(jiàn)表1。
表1 PCR擴增上游和下游引物核酸序列
|
基因名稱(chēng) |
上游引物5’-3’ |
下游引物5’-3’ |
|
SOCS-3 |
TCACCCACAGCAAGTTTCC |
GGATGCGTAGGTTCTTGGTC |
|
PPARγ |
TTGATTTCTCCAGCATTTC |
TTCAATCGGATGTTCTT |
|
ACO |
GCCCTCAGCTATGGTATTAC |
AGGAACTGCTCTCACAATGC |
|
β-actin |
TTGTAACCAACTGGGACGATATGG |
GATCTTGATCTTCATGGTGCTAGG |
1.4 統計分析
全部結果以均數±標準差表示,并采用SPSS13.0 軟件進(jìn)行統計分析。
2 結果
2.1 飼養期內對照組和肥胖組大鼠體重變化
給予高脂飼料前,對照組(185.83±5.74)g和肥胖組大鼠體重(184.13±13.38)g差異無(wú)顯著(zhù)性(P>0.05),但從第3周體重開(kāi)始分化,到第4周末,喂飼高脂飼料的肥胖組大鼠體重顯著(zhù)高于對照組(P<0.05)。此后,肥胖組大鼠體重一直高于對照組,至第8周末,肥胖組大鼠體重達(413.13±70.5)g,顯著(zhù)高于對照組大鼠體重(332±54.74)g,且體重增量為(229±64.54)g,顯著(zhù)高于對照組大鼠體重增量(146.17±50.72)g (P<0.05) (圖1)。
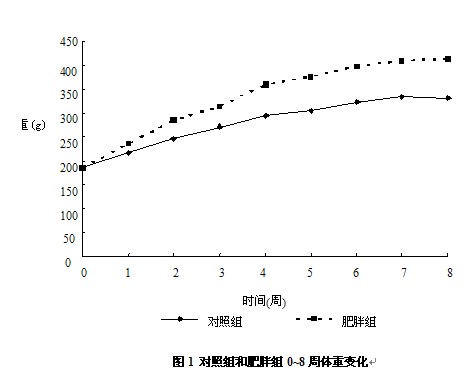
2.2 第8周末大鼠腹部脂肪儲存狀況和血清瘦素水平比較
實(shí)驗結束時(shí),肥胖組大鼠腸系膜、腎周、附睪脂肪組織重量、總脂肪均顯著(zhù)高于對照組,血清瘦素水平也顯著(zhù)高于對照組(表2)。
表2 對照組和肥胖組大鼠腹部脂肪儲存狀況和血清瘦素水平
Table 2 The abdomen fat and serum leptin level in control and obese group(`x±s)
|
組別 |
腸系膜
(g) |
腎周
(g) |
附睪
(g) |
總脂肪
(g) |
瘦素
(ng/ml) |
|
對照組 |
0.90±0.49 |
1.88±0.76 |
3.63±0.96 |
6.41±2.04 |
0.48±0.29 |
|
肥胖組 |
2.99±1.63(1) |
5.43±1.64(2) |
7.79±2.11(2) |
16.21±4.93(2) |
0.95±0.42(1) |
注:(1)與對照組比較 P<0.05,(2)與對照組比較P<0.01
2.3第8周末對照組和肥胖組大鼠SOCS-3,PPARγ、ACOmRNA表達情況
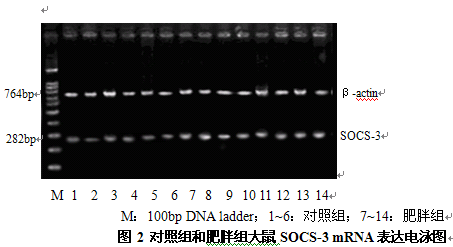
M:100bp DNA ladder;1~6:對照組;7~14:肥胖組
圖2 對照組和肥胖組大鼠SOCS-3 mRNA表達電泳圖

圖3對照組和肥胖組大鼠PPARγ mRNA表達電泳圖
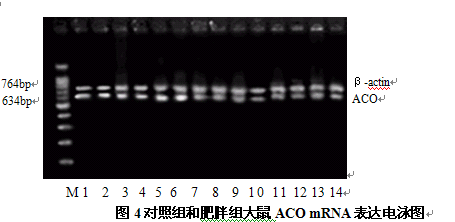
圖4對照組和肥胖組大鼠ACO mRNA表達電泳圖
表3 對照組和肥胖組大鼠SOCS-3、PPARγ、ACOmRNA灰度值分析
Table 3 SOCS-3,PPARγ and ACO mRNA level in control and obese group
|
組別 |
例數 |
SOCS-3 |
PPARγ |
ACO |
|
對照組 |
6 |
0.66±0.11 |
0.37±0.12 |
1.08±0.17 |
|
肥胖組 |
8 |
0.94±0.21(1) |
0.57±0.13(1) |
0.72±0.11(2) |
注:(1) 與對照組比較 P<0.05,(2) 與對照組比較 P<0.01
由圖2、圖3可見(jiàn),肥胖組大鼠的SOCS-3 mRNA、PPARγ mRNA表達水平高于對照組,圖4顯示肥胖組大鼠的ACO mRNA表達水平低于對照組,灰度值分析結果顯示其差異具有統計學(xué)顯著(zhù)性(P<0.05,P<0.01)。
3 討論
瘦素抵抗是指體內存在高瘦素血癥以及對瘦素減少體重的信號反應能力降低[1]。大多數肥胖的人和嚙齒類(lèi)動(dòng)物存在瘦素抵抗現象,本實(shí)驗采用高脂膳食成功誘導了Wistar肥胖大鼠模型,并通過(guò)檢測血清瘦素水平,證實(shí)肥胖組大鼠存在瘦素抵抗,即肥胖組大鼠體重和脂肪墊重量顯著(zhù)高于對照組,而血清瘦素水平也顯著(zhù)高于對照組。瘦素抵抗的產(chǎn)生機制有多種,其中瘦素在中樞和外周的信號轉導通路缺陷,形成瘦素信號的轉導抑制物增多是產(chǎn)生瘦素抵抗的重要機制。SOCS-3是瘦素信號轉導的負反饋抑制因子[2,3]。它可以由瘦素誘導產(chǎn)生,該過(guò)程需要Jak/STAT通路的參與,而誘導產(chǎn)生的SOCS-3通過(guò)與Jak結合而抑制了Jak的酪氨酸激酶活性及Jak誘導的瘦素受體的酪氨酸磷酸化,從而抑制了瘦素受體后的Jak/STAT信號轉導通路。瘦素發(fā)揮調節體重的作用不僅通過(guò)下丘腦的瘦素受體,而且也通過(guò)與脂肪細胞的OB-Rb結合,激活Jak/STAT信號轉導通路,對脂肪細胞發(fā)揮直接的自分泌或旁分泌作用,引起脂肪減少,體重降低[4,5]。本研究顯示肥胖組大鼠脂肪組織SOCS-3 mRNA 表達顯著(zhù)高于對照組,提示高脂飲食誘導的肥胖大鼠存在外周瘦素信號轉導通路的抑制。
同時(shí)我們檢測了脂肪組織中PPARγ和ACO 的mRNA表達,結果顯示肥胖組PPAPγ mRNA表達水平顯著(zhù)高于對照組,ACO mRNA水平則顯著(zhù)低于對照組。PPARγ是一類(lèi)由配體激活的核轉錄因子,為核激素受體超家族中的成員,也是脂質(zhì)活化的轉錄因子,在調節胰島素作用、脂質(zhì)代謝與糖代謝、脂肪細胞分化和能量平衡方面起重要的調節作用。PPARγ mRNA表達增加,會(huì )起到上調脂肪合成酶如乙酰輔酶A羧化酶、脂肪酸合成酶及甘油三磷酸轉乙酰酶的作用,促進(jìn)脂肪的合成。而ACO是脂肪細胞內與脂肪酸氧化相關(guān)的酶,肥胖大鼠該酶降低,提示肥胖大鼠存在瘦素抵抗的同時(shí),脂肪組織內脂肪酸氧化能力也降低,促使脂肪細胞的脂肪儲存進(jìn)一步增加。
本研究顯示高脂飲食誘導的肥胖大鼠血清瘦素水平增加,脂肪組織SOCS-3、ACO mRNA水平增加,而PPARγ mRNA水平降低,提示肥胖大鼠可能存在外周的瘦素抵抗,脂肪酸氧化能力降低,脂肪合成能力增強。但關(guān)于肥胖、瘦素抵抗及影響脂肪合成和分解的相關(guān)因子、酶類(lèi)之間的內在作用機制,它們之間是否存在相互影響還需進(jìn)一步探討。
參考文獻
1 EL-HASCHIMI K, PIERROZ D D, HILEMAN S M, et al. Two defects contribute to hypothalamic leptin resistance in mice with diet-induced obesity[J]. J Clin Invest, 2000,105(12):1827-1832.
2 BJORBAEK C, EL-HASCHIMI K, FRANTZ J D, et al. The role of SOCS-3 in leptin signaling and leptin resistance [J]. J Biol Chem, 1999,274(2):30059-30065.
3 MUNZBERG H, FLIER J S, BJORBAEK C. Region-specific leptin resistance within the hypothalamus of diet-induced obese mice [J]. Endocrinology, 2004,145(11):4880-4889.
4 MINOLOSHI Y, KIM Y B, PERONI O D, et al. Leptin stimulates fatty acid oxidation by activating AMP-activated protein kinase [J]. Nature, 2002,415(6869):339-343.
5 ATKINSON L L, FISCHER M A, LOPASCHUK G D. Leptin activates cardiac fatty acid oxidation independent of changes in the AMP-activated protein kinase: acetyl-CoA carboxylase-malonyl- CoA axis [J]. J Biol Chem, 2002,277(33):29424-29430.
收稿日期:2007-06-05
